વૃદ્ધોમાં જોવા મળતો સૌથી સામાન્ય રોગ, અલ્ઝાઇમર રોગ, મોટાભાગના લોકોને સતાવી રહ્યો છે.
અલ્ઝાઇમર રોગની સારવારમાં એક પડકાર એ છે કે મગજના પેશીઓમાં ઉપચારાત્મક દવાઓનો પુરવઠો રક્ત-મગજ અવરોધ દ્વારા મર્યાદિત છે. અભ્યાસમાં જાણવા મળ્યું છે કે MRI-માર્ગદર્શિત ઓછી-તીવ્રતા કેન્દ્રિત અલ્ટ્રાસાઉન્ડ અલ્ઝાઇમર રોગ અથવા પાર્કિન્સન રોગ, મગજની ગાંઠો અને એમીયોટ્રોફિક લેટરલ સ્ક્લેરોસિસ સહિત અન્ય ન્યુરોલોજીકલ વિકૃતિઓ ધરાવતા દર્દીઓમાં રક્ત-મગજ અવરોધને ઉલટાવી શકે છે.
વેસ્ટ વર્જિનિયા યુનિવર્સિટી ખાતે રોકફેલર ઇન્સ્ટિટ્યૂટ ફોર ન્યુરોસાયન્સમાં તાજેતરમાં કરવામાં આવેલા એક નાના પ્રૂફ-ઓફ-કન્સેપ્ટ ટ્રાયલમાં દર્શાવવામાં આવ્યું છે કે અલ્ઝાઇમર રોગના દર્દીઓ જેમણે ફોકસ્ડ અલ્ટ્રાસાઉન્ડ સાથે એડ્યુકેનુમાબ ઇન્ફ્યુઝન મેળવ્યું હતું, તેમણે બ્લડ-બ્રેઇન બેરિયરને અસ્થાયી રૂપે ખોલ્યું હતું, જેનાથી ટ્રાયલ બાજુ પર મગજ એમીલોઇડ બીટા (Aβ) લોડમાં નોંધપાત્ર ઘટાડો થયો હતો. આ સંશોધન મગજના વિકારોની સારવાર માટે નવા દરવાજા ખોલી શકે છે.
રક્ત-મગજ અવરોધ મગજને હાનિકારક પદાર્થોથી રક્ષણ આપે છે જ્યારે આવશ્યક પોષક તત્વોને પસાર થવા દે છે. પરંતુ રક્ત-મગજ અવરોધ મગજમાં ઉપચારાત્મક દવાઓના વિતરણને પણ અટકાવે છે, જે અલ્ઝાઇમર રોગની સારવાર કરતી વખતે ખાસ કરીને તીવ્ર પડકાર છે. જેમ જેમ વિશ્વ વૃદ્ધ થાય છે તેમ, અલ્ઝાઇમર રોગ ધરાવતા લોકોની સંખ્યા દર વર્ષે વધી રહી છે, અને તેના સારવાર વિકલ્પો મર્યાદિત છે, જે આરોગ્યસંભાળ પર ભારે બોજ નાખે છે. એડ્યુકેનુમાબ એ એમીલોઇડ બીટા (Aβ)-બંધનકર્તા મોનોક્લોનલ એન્ટિબોડી છે જેને અલ્ઝાઇમર રોગની સારવાર માટે યુએસ ફૂડ એન્ડ ડ્રગ એડમિનિસ્ટ્રેશન (FDA) દ્વારા મંજૂર કરવામાં આવ્યું છે, પરંતુ રક્ત-મગજ અવરોધમાં તેનો પ્રવેશ મર્યાદિત છે.
કેન્દ્રિત અલ્ટ્રાસાઉન્ડ યાંત્રિક તરંગો ઉત્પન્ન કરે છે જે સંકોચન અને મંદન વચ્ચેના ઓસિલેશનને પ્રેરિત કરે છે. જ્યારે લોહીમાં ઇન્જેક્ટ કરવામાં આવે છે અને અલ્ટ્રાસોનિક ક્ષેત્રના સંપર્કમાં આવે છે, ત્યારે પરપોટા આસપાસના પેશીઓ અને લોહી કરતાં વધુ સંકુચિત અને વિસ્તરે છે. આ ઓસિલેશન રક્ત વાહિની દિવાલ પર યાંત્રિક તાણ બનાવે છે, જેના કારણે એન્ડોથેલિયલ કોષો વચ્ચેના ચુસ્ત જોડાણો ખેંચાય છે અને ખુલે છે (નીચેની આકૃતિ). પરિણામે, રક્ત-મગજ અવરોધની અખંડિતતા જોખમાય છે, જેનાથી અણુઓ મગજમાં ફેલાય છે. રક્ત-મગજ અવરોધ લગભગ છ કલાકમાં તેની જાતે જ સાજો થઈ જાય છે.
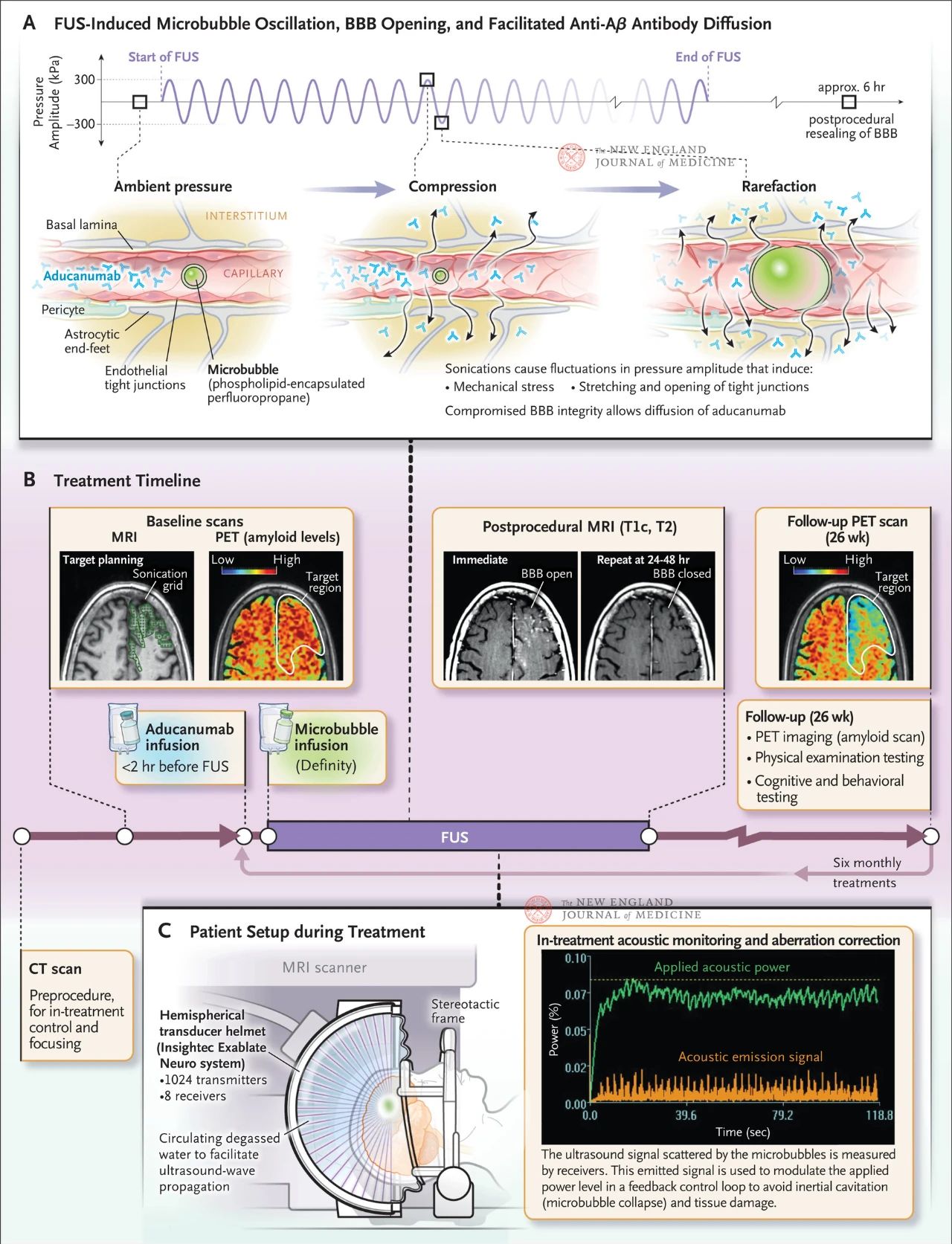
આકૃતિ રક્ત વાહિનીઓમાં માઇક્રોમીટર-કદના પરપોટા હાજર હોય ત્યારે રુધિરકેશિકાઓની દિવાલો પર દિશાત્મક અલ્ટ્રાસાઉન્ડની અસર દર્શાવે છે. ગેસની ઉચ્ચ સંકોચનક્ષમતાને કારણે, પરપોટા આસપાસના પેશીઓ કરતાં વધુ સંકોચાય છે અને વિસ્તરે છે, જેના કારણે એન્ડોથેલિયલ કોષો પર યાંત્રિક તાણ આવે છે. આ પ્રક્રિયાને કારણે ચુસ્ત જોડાણો ખુલે છે અને એસ્ટ્રોસાઇટના અંત રક્ત વાહિનીઓની દિવાલ પરથી પડી શકે છે, જે રક્ત-મગજ અવરોધની અખંડિતતા સાથે સમાધાન કરે છે અને એન્ટિબોડી પ્રસારને પ્રોત્સાહન આપે છે. વધુમાં, કેન્દ્રિત અલ્ટ્રાસાઉન્ડના સંપર્કમાં આવતા એન્ડોથેલિયલ કોષોએ તેમની સક્રિય વેક્યુલર પરિવહન પ્રવૃત્તિમાં વધારો કર્યો અને પ્રવાહ પંપ કાર્યને દબાવ્યું, જેનાથી મગજમાં એન્ટિબોડીઝની મંજૂરી ઓછી થઈ. આકૃતિ B સારવાર સમયપત્રક દર્શાવે છે, જેમાં અલ્ટ્રાસાઉન્ડ સારવાર યોજના વિકસાવવા માટે કમ્પ્યુટેડ ટોમોગ્રાફી (CT) અને મેગ્નેટિક રેઝોનન્સ ઇમેજિંગ (MRI), બેઝલાઇન પર 18F-ફ્લુબિટાબન પોઝિટ્રોન એમિશન ટોમોગ્રાફી (PET), કેન્દ્રિત અલ્ટ્રાસાઉન્ડ સારવાર પહેલાં એન્ટિબોડી ઇન્ફ્યુઝન અને સારવાર દરમિયાન માઇક્રોવેસિક્યુલર ઇન્ફ્યુઝન, અને સારવારને નિયંત્રિત કરવા માટે ઉપયોગમાં લેવાતા માઇક્રોવેસિક્યુલર સ્કેટરિંગ અલ્ટ્રાસાઉન્ડ સિગ્નલોનું એકોસ્ટિક મોનિટરિંગ શામેલ છે. ફોકસ્ડ અલ્ટ્રાસાઉન્ડ ટ્રીટમેન્ટ પછી મેળવેલી છબીઓમાં T1-વેઇટેડ કોન્ટ્રાસ્ટ-એન્હાન્સ્ડ MRIનો સમાવેશ થાય છે, જે દર્શાવે છે કે અલ્ટ્રાસાઉન્ડ ટ્રીટેડ એરિયામાં બ્લડ-બ્રેઇન બેરિયર ખુલ્લું હતું. ફોકસ્ડ અલ્ટ્રાસાઉન્ડ ટ્રીટમેન્ટના 24 થી 48 કલાક પછી તે જ વિસ્તારની છબીઓમાં બ્લડ-બ્રેઇન બેરિયરનો સંપૂર્ણ રૂઝ આવવાનો સંકેત મળ્યો. 26 અઠવાડિયા પછી એક દર્દીમાં ફોલો-અપ દરમિયાન 18F-ફ્લુબિટાબેન PET સ્કેન કરવામાં આવ્યું જેમાં સારવાર પછી મગજમાં Aβ સ્તરમાં ઘટાડો જોવા મળ્યો. આકૃતિ C સારવાર દરમિયાન MRI-માર્ગદર્શિત ફોકસ્ડ અલ્ટ્રાસાઉન્ડ સેટઅપ દર્શાવે છે. હેમિસ્ફેરિકલ ટ્રાન્સડ્યુસર હેલ્મેટમાં 1,000 થી વધુ અલ્ટ્રાસાઉન્ડ સ્ત્રોતો છે જે MRI ના રીઅલ-ટાઇમ માર્ગદર્શનનો ઉપયોગ કરીને મગજમાં એક જ ફોકલ પોઈન્ટ પર ભેગા થાય છે.
2001 માં, પ્રાણીઓના અભ્યાસોમાં ફોકસ્ડ અલ્ટ્રાસાઉન્ડ રક્ત-મગજ અવરોધ ખોલવા માટે સૌપ્રથમ દર્શાવવામાં આવ્યું હતું, અને ત્યારબાદના પ્રીક્લિનિકલ અભ્યાસોએ દર્શાવ્યું છે કે ફોકસ્ડ અલ્ટ્રાસાઉન્ડ દવા પહોંચાડવા અને અસરકારકતામાં વધારો કરી શકે છે. ત્યારથી, એવું જાણવા મળ્યું છે કે ફોકસ્ડ અલ્ટ્રાસાઉન્ડ અલ્ઝાઈમરના દર્દીઓમાં બ્લડ-મગજ અવરોધને સુરક્ષિત રીતે ખોલી શકે છે જેઓ દવા લેતા નથી, અને સ્તન કેન્સર મગજ મેટાસ્ટેસિસ માટે એન્ટિબોડીઝ પણ પહોંચાડી શકે છે.
માઇક્રોબબલ ડિલિવરી પ્રક્રિયા
માઇક્રોબબલ્સ એક અલ્ટ્રાસાઉન્ડ કોન્ટ્રાસ્ટ એજન્ટ છે જેનો ઉપયોગ સામાન્ય રીતે અલ્ટ્રાસાઉન્ડ નિદાનમાં રક્ત પ્રવાહ અને રક્ત વાહિનીઓનું નિરીક્ષણ કરવા માટે થાય છે. અલ્ટ્રાસાઉન્ડ થેરાપી દરમિયાન, ઓક્ટાફ્લોરોપ્રોપેનનું ફોસ્ફોલિપિડ-કોટેડ નોન-પાયરોજેનિક બબલ સસ્પેન્શન નસમાં ઇન્જેક્ટ કરવામાં આવ્યું હતું (આકૃતિ 1B). માઇક્રોબબલ્સ ખૂબ જ પોલીડિસ્પર્સ્ડ હોય છે, જેનો વ્યાસ 1 μm કરતા ઓછા થી 10 μm કરતા વધુ હોય છે. ઓક્ટાફ્લોરોપ્રોપેન એક સ્થિર ગેસ છે જે ચયાપચય થતો નથી અને ફેફસાં દ્વારા ઉત્સર્જન કરી શકાય છે. લિપિડ શેલ જે પરપોટાને લપેટે છે અને સ્થિર કરે છે તે ત્રણ કુદરતી માનવ લિપિડ્સથી બનેલું છે જે એન્ડોજેનસ ફોસ્ફોલિપિડ્સની જેમ જ ચયાપચય થાય છે.
કેન્દ્રિત અલ્ટ્રાસાઉન્ડનું ઉત્પાદન
દર્દીના માથાને ઘેરી લેનારા હેમિસ્ફેરિકલ ટ્રાન્સડ્યુસર હેલ્મેટ દ્વારા ફોકસ્ડ અલ્ટ્રાસાઉન્ડ ઉત્પન્ન થાય છે (આકૃતિ 1C). હેલ્મેટ 1024 સ્વતંત્ર રીતે નિયંત્રિત અલ્ટ્રાસાઉન્ડ સ્ત્રોતોથી સજ્જ છે, જે કુદરતી રીતે ગોળાર્ધના કેન્દ્રમાં કેન્દ્રિત છે. આ અલ્ટ્રાસાઉન્ડ સ્ત્રોતો સાઇનુસોઇડલ રેડિયો-ફ્રીક્વન્સી વોલ્ટેજ દ્વારા ચલાવવામાં આવે છે અને મેગ્નેટિક રેઝોનન્સ ઇમેજિંગ દ્વારા સંચાલિત અલ્ટ્રાસોનિક તરંગો ઉત્સર્જિત કરે છે. દર્દી હેલ્મેટ પહેરે છે અને અલ્ટ્રાસાઉન્ડ ટ્રાન્સમિશનને સરળ બનાવવા માટે ગેસ મુક્ત પાણી માથાની આસપાસ ફરે છે. અલ્ટ્રાસાઉન્ડ ત્વચા અને ખોપરી દ્વારા મગજના લક્ષ્ય સુધી પ્રવાસ કરે છે.
ખોપરીની જાડાઈ અને ઘનતામાં ફેરફાર અલ્ટ્રાસાઉન્ડ પ્રસારને અસર કરશે, જેના પરિણામે અલ્ટ્રાસાઉન્ડને જખમ સુધી પહોંચવામાં થોડો અલગ સમય મળશે. ખોપરીના આકાર, જાડાઈ અને ઘનતા વિશે માહિતી મેળવવા માટે ઉચ્ચ-રિઝોલ્યુશન કમ્પ્યુટેડ ટોમોગ્રાફી ડેટા મેળવીને આ વિકૃતિ સુધારી શકાય છે. કમ્પ્યુટર સિમ્યુલેશન મોડેલ તીક્ષ્ણ ફોકસને પુનઃસ્થાપિત કરવા માટે દરેક ડ્રાઇવ સિગ્નલના વળતર તબક્કા શિફ્ટની ગણતરી કરી શકે છે. RF સિગ્નલના તબક્કાને નિયંત્રિત કરીને, અલ્ટ્રાસાઉન્ડને ઇલેક્ટ્રોનિક રીતે ફોકસ કરી શકાય છે અને અલ્ટ્રાસાઉન્ડ સ્રોત એરેને ખસેડ્યા વિના મોટી માત્રામાં પેશીઓને આવરી લેવા માટે સ્થિત કરી શકાય છે. હેલ્મેટ પહેરતી વખતે માથાના ચુંબકીય રેઝોનન્સ ઇમેજિંગ દ્વારા લક્ષ્ય પેશીઓનું સ્થાન નક્કી કરવામાં આવે છે. લક્ષ્ય વોલ્યુમ અલ્ટ્રાસોનિક એન્કર પોઇન્ટ્સના ત્રિ-પરિમાણીય ગ્રીડથી ભરવામાં આવે છે, જે દરેક એન્કર પોઇન્ટ પર 5-10 ms માટે અલ્ટ્રાસોનિક તરંગો ઉત્સર્જન કરે છે, દર 3 સેકન્ડે પુનરાવર્તિત થાય છે. ઇચ્છિત બબલ સ્કેટરિંગ સિગ્નલ શોધી કાઢવામાં ન આવે ત્યાં સુધી અલ્ટ્રાસોનિક પાવર ધીમે ધીમે વધારવામાં આવે છે, અને પછી 120 સેકન્ડ માટે રાખવામાં આવે છે. લક્ષ્ય વોલ્યુમ સંપૂર્ણપણે આવરી લેવામાં ન આવે ત્યાં સુધી આ પ્રક્રિયા અન્ય મેશ પર પુનરાવર્તિત થાય છે.
રક્ત-મગજ અવરોધ ખોલવા માટે ધ્વનિ તરંગોનું કંપનવિસ્તાર ચોક્કસ થ્રેશોલ્ડ કરતાં વધુ હોવું જરૂરી છે, જે પેશીને નુકસાન થાય ત્યાં સુધી વધતા દબાણ કંપનવિસ્તાર સાથે અવરોધની અભેદ્યતા વધે છે, જે એરિથ્રોસાઇટ એક્સોસ્મોસિસ, રક્તસ્રાવ, એપોપ્ટોસિસ અને નેક્રોસિસ તરીકે પ્રગટ થાય છે, જે બધા ઘણીવાર બબલ પતન (જેને ઇનર્શિયલ પોલાણ કહેવાય છે) સાથે સંકળાયેલા હોય છે. થ્રેશોલ્ડ માઇક્રોબબલના કદ અને શેલ સામગ્રી પર આધાર રાખે છે. માઇક્રોબબલ્સ દ્વારા વિખેરાયેલા અલ્ટ્રાસોનિક સિગ્નલોને શોધી અને અર્થઘટન કરીને, એક્સપોઝરને સુરક્ષિત શ્રેણીમાં રાખી શકાય છે.
અલ્ટ્રાસાઉન્ડ સારવાર પછી, લક્ષ્ય સ્થાન પર રક્ત-મગજ અવરોધ ખુલ્લો છે કે નહીં તે નક્કી કરવા માટે કોન્ટ્રાસ્ટ એજન્ટ સાથે T1-ભારિત MRI નો ઉપયોગ કરવામાં આવ્યો હતો, અને T2-ભારિત છબીઓનો ઉપયોગ એક્સ્ટ્રાવેઝેશન અથવા રક્તસ્ત્રાવ થયો છે કે કેમ તેની પુષ્ટિ કરવા માટે કરવામાં આવ્યો હતો. જો જરૂરી હોય તો, આ અવલોકનો અન્ય સારવારોને સમાયોજિત કરવા માટે માર્ગદર્શન પૂરું પાડે છે.
મૂલ્યાંકન અને રોગનિવારક અસરની સંભાવના
સંશોધકોએ સારવાર પહેલા અને પછી 18F-ફ્લુબિટાબેન પોઝિટ્રોન ઉત્સર્જન ટોમોગ્રાફીની તુલના કરીને મગજ Aβ લોડ પર સારવારની અસરનું પ્રમાણ નક્કી કર્યું જેથી સારવાર કરાયેલ વિસ્તાર અને વિરુદ્ધ બાજુના સમાન વિસ્તાર વચ્ચે Aβ વોલ્યુમમાં તફાવતનું મૂલ્યાંકન કરી શકાય. આ જ ટીમ દ્વારા અગાઉના સંશોધનોએ દર્શાવ્યું છે કે ફક્ત અલ્ટ્રાસાઉન્ડ પર ધ્યાન કેન્દ્રિત કરવાથી Aβ સ્તર થોડું ઓછું થઈ શકે છે. આ ટ્રાયલમાં જોવા મળેલો ઘટાડો અગાઉના અભ્યાસો કરતા પણ વધારે હતો.
ભવિષ્યમાં, મગજની બંને બાજુ સારવારનો વિસ્તાર કરવો એ રોગની પ્રગતિમાં વિલંબ કરવામાં તેની અસરકારકતાનું મૂલ્યાંકન કરવા માટે મહત્વપૂર્ણ રહેશે. વધુમાં, લાંબા ગાળાની સલામતી અને અસરકારકતા નક્કી કરવા માટે વધુ સંશોધનની જરૂર છે, અને વ્યાપક ઉપલબ્ધતા માટે ઓનલાઈન MRI માર્ગદર્શન પર આધાર રાખતા ન હોય તેવા ખર્ચ-અસરકારક ઉપચારાત્મક ઉપકરણો વિકસાવવા જોઈએ. તેમ છતાં, તારણોએ આશાવાદ જગાવ્યો છે કે Aβ ને સાફ કરતી સારવાર અને દવાઓ આખરે અલ્ઝાઈમરની પ્રગતિને ધીમી કરી શકે છે.
પોસ્ટ સમય: જાન્યુઆરી-06-2024